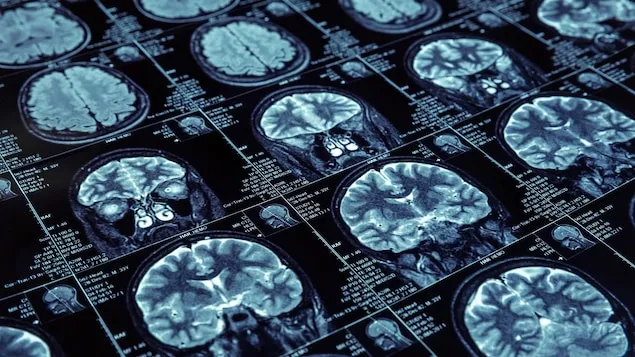
新药通过静脉注射,针对大脑中堆积的致病粘性淀粉样斑块(sticky amyloid plaque)。照片:GETTY IMAGES/ISTOCKPHOTO / NOMADSOUL1
礼来公司(Eli Lilly)的 Kisunla,用于治疗阿尔茨海默氏症引起的轻度或早期失智症(前称痴呆症)。这是继去年日本制药商卫采(Eisai)一种类似药物获批后的新一种获批药物。
两种药物可延缓病情几个月,Kinsula的延缓期约为七个月。
虽然有帮助,但药物须定期进行静脉注射,另外也有潜在副作用如脑肿胀,因此患者及家属亦必须权衡风险。
减缓衰退
Kisunla和日本药物Leqembi,都是实验室制造出来的抗体,通过静脉注射,针对大脑中堆积的致病粘性淀粉样斑块(sticky amyloid plaque)。
化学名称为多那尼单抗Donanemab的Kisunla,获批依据是一项为期18个月的研究结果。在研究中,接受治疗的患者,在记忆和认知能力方面的下降速度,比接受假注射的患者慢了22%。
加拿大阿尔茨海默氏症协会(Alzheimer Society of Canada)称,2030年的失智症患者总人数预计将會有100万。
惟目前加拿大卫生部并未批准使用Kisunla和Leqembi。
药物的主要安全性风险是脑肿胀和出血,这是所有斑块标靶药的共同问题。
礼来公司的研究报告显示包括微出血等出血问题机会为20%,略高于竞争对手Leqembi。但两药进行测试的患者略微不同,因此难以直接比较安全性。
每月输液一次
Kisunla服用者须每月输液一次,而Leqembi则为每月两次。另外,Kisunla使用者如果反应良好,可以停止服用。
在Kisunla药物研究中,超过四成患者在一年后停止服药。但研究未有说明患者何时需要恢复用药。
惟要用药,医生需要先确认患者是否有新药所针对的脑斑块。另外,在进行注射之余,护理人员亦必须反复扫描,以检查患者脑部是否肿胀或出血。
礼来公司将Kisunla定价为每瓶695.65美元。
The Associated Press, avec les informations de Reuters et CBC News. Adaptation en chinois par Donna Chan.